Метаболический синдром - (синдром Reaven) представляет собой симптомокомплекс, сочетающий в себе абдоминальное ожирение, инсулинорезистентность, гипергликемию (повышенное содержание глюкозы в крови), дислипидемию и артериальную гипертензию
Все эти нарушения связаны в одну патогенетическую цепь. Кроме того, такой синдром часто сочетается с гиперурикемией (избытком мочевой кислоты в крови), нарушением гемостаза (свёртываемости крови), субклиническим воспалением, синдромом обструктивного апноэ-гипопноэ сна (остановкой дыхания во сне).
Метаболический синдром у женщин репродуктивного возраста ранее практикующие врачи знали как нейрообменноэндокринный синдром, протекающий по типу лёгкой формы болезни Кушинга, гипоталамический или диэнцефальный синдром. В данной статье материал будет представлен с позиций гинеколога-эндокринолога. У женщин репродуктивного возраста метаболический синдром — одна из наиболее частых причин нарушения репродуктивной функции на фоне прогрессирующего ожирения и диэнцефальной симптоматики.
ЭПИДЕМИОЛОГИЯ
Частота данной патологии составляет в популяции до 15–20%, примерно 30–35% в структуре нарушений репродуктивной функции и до 70% среди женщин с рецидивирующими гиперпластическими процессами эндометрия; частота ранних потерь беременности при данном синдроме возрастает до 35%.
ЭТИОЛОГИЯ
Причины развития метаболического синдрома - воздействие различных факторов (психические стрессы, нейроинфекции, различные операции, травмы, роды, аборты и др.) у женщин с определённым преморбидным фоном (врождённая или приобретённая функциональная лабильность гипоталамических и экстрагипоталамических структур).
ПАТОГЕНЕЗ
Первично происходит нарушение нейроэндокринной регуляции гипоталамуса, поэтому отмечается множество диэнцефальных симптомов (нарушение сна, аппетита, жажда, головокружения, головные боли, гипертензия и др.), указывающих на центральный (гипоталамический) генез данной патологии. В ответ на воздействие различных этиологических факторов (стресс) в экстрагипоталамических структурах мозга происходит нарушение обмена нейромедиаторов, в частности увеличение синтеза и выделения β-эндорфина и уменьшение продукции допамина.
Вследствие этого повышается секреция АКТГ, пролактина, нарушается цирхоральный ритм выделения гонадолиберина и, соответственно, гонадотропинов в гипофизе. Внегонадно синтезирующийся из андрогенов эстрон повышает чувствительность гипофиза к гонадолиберину, что дополнительно нарушает функцию гипоталамо-гипофизарно-яичниковой системы с формированием вторичных поликистозных яичников. Нарушения в системе гипоталамус-гипофиз-надпочечники. В ответ на избыточную стимуляцию АКТГ в надпочечниках повышается образование всех стероидных гормонов коры: глюкокортикоидов (кортизол), минералокортикоидов (альдостерон) и половых гормонов, в основном андрогенов. Гиперкортицизм способствует специфическому, так называемому висцеральному ожирению (центральное, кушингоидное, мужское, андроидное ожирение) с преимущественным отложением жировой ткани в области плечевого пояса, живота и мезентерия внутренних органов.
Висцеральная жировая ткань приводит к формированию инсулинорезистентности вследствие гиперинсулинемии. Затем происходит нарушение липидного спектра крови (дислипидемия), характеризующаяся повышением уровня атерогенных факторов (триглицеридов, липопротеидов низкой плотности, липопротеидов очень низкой плотности) и снижением уровня липопротеидов высокой плотности, что приводит к атеросклерозу и артериальной гипертонии. При этом последовательность развития метаболических нарушений соответствует длительности заболевания. Поэтому артериальная гипертония, обязательный компонент метаболического синдрома, проявляется, как правило, после 35 лет.
Висцеральному ожирению также способствует булимия (повышенный аппетит и избыточное потребление пищи) вследствие нарушения нейромедиаторного контроля за функцией центров пищевого поведения, находящихся в гипоталамусе. Периферической инсулинорезистентности также способствуют надпочечниковые андрогены и тестостерон, продуцирующийся в жировой ткани. Известно, что андрогены изменяют структуру мышечной ткани в сторону превалирования мышечных волокон II типа, менее чувствительных к инсулину. Таким образом, в результате активации оси «гипоталамус-гипофиз-надпочечники» формируются 4 основные компонента («смертельный квартет») метаболического синдрома: висцеральное ожирение, инсулинорезистентность, дислипидемия и артериальная гипертония.
Чёткой классификации и стадийности метаболического синдрома не существует. Несмотря на это, выраженность симптомов, количество компонентов синдрома Reaven и наличие осложнений оказывают влияние на стратификацию риска и выбор тактики лечения у конкретного пациента. Для этого следует учитывать:
• степень ожирения и артериальной гипертензии;
• выраженность метаболических изменений;
• наличие или отсутствие сахарного диабета и заболеваний, связанных с атеросклерозом.
В зависимости от индекса массы тела (ИМТ), который рассчитывается делением веса (кг) на рост (м2), классифицируются следующие типы массы тела (МТ):
• нормальная МТ — ИМТ ≥18,5 <25;
• избыточная МТ — ≥25 <30;
• ожирение I степени — ≥30 <35;
• ожирение II степени — ≥35 <40;
• ожирение III степени — ≥40.
ИМТ <18,5 характеризуется как дефицит массы тела.
Важную роль играет распределение жировой ткани. Различают два типа ожирения:
• гиноидный (по типу «груша»), когда избыточная жировая ткань распределяется преимущественно на бёдрах и ягодицах;
• андроидный (по типу «яблоко»; абдоминальное ожирение), с преимущественной локализацией жира в области верхней половины тела (живот, грудь, плечи, спина).
Второй тип ожирения является более патогенным в плане риска возникновения сердечно-сосудистых заболеваний и сахарного диабета. Это связано с ожирением внутренних органов, в том числе печени (висцеральное ожирение, неалкогольная жировая болезнь печени), снижением сатурации крови кислородом из-за перехода дыхания на грудной, поверхностный тип и эндокринной активностью висцеральной жировой ткани с патологическим изменением выработки адипокинов (лептин, грелин, адипонектин). Выявлена чёткая корреляция между увеличением абдоминальной жировой ткани и индекса массы тела с риском сопутствующих заболеваний. Считается, что риски начинают нарастать при увеличении окружности талии (ОТ) >80 см у женщин и 94 см у мужчин, а при ОТ >88 см и 102 см соответственно риск возрастает значительно.
Центральным патологическим звеном метаболического синдрома является изменение углеводного обмена. Концентрацию глюкозы оценивают в капиллярной крови (норма <5,6) и в венозной плазме (норма <6,1) натощак в ммоль/л. Гипергликемией натощак считается показатель ≥5,6 <6,1 и ≥6,1; <7,0; сахарный диабет — ≥6,1 и ≥6,1 <7,0, соответственно. Через 2 часа после углеводной нагрузки (75 гр глюкозы или 125 гр сахара рафинада, растворённых в 200 мл воды) нормальный показатель концентрации глюкозы в капиллярной и венозной крови — <7,8 ммоль/л; НТГ — ≥7,8 <11,1 и сахарный диабет — ≥11,1.
Ещё один важный компонент метаболического синдрома — артериальная гипертензия, которая может носить вторичный характер. Нормальным считается систолическое артериальное давление (САД) 120-129 мм рт.ст и диастолическое артериальное давление (ДАД) 80-84 мм рт.ст. САД <120 и ДАД <80 называют оптимальным давлением, а САД 130-139 и ДАД 85-89 — высоким нормальным артериальным давлением.
Различают три степени артериальной гипертензии:
• 1 ст. – САД 140-159, ДАД 90-99;
• 2 ст. - САД 160-179, ДАД 100-109;
• 3 ст. - САД ≥180, ДАД ≥110.
Повышение артериального давления характеризуется повышением риска сердечно-сосудистых событий. Для метаболического синдрома характерны также изменения липидного обмена, которые классифицированы в таблице ниже (в ммоль/л).
Метаболический синдром у женщин репродуктивного возраста ранее практикующие врачи знали как нейрообменноэндокринный синдром, протекающий по типу лёгкой формы болезни Кушинга, гипоталамический или диэнцефальный синдром. В данной статье материал будет представлен с позиций гинеколога-эндокринолога. У женщин репродуктивного возраста метаболический синдром — одна из наиболее частых причин нарушения репродуктивной функции на фоне прогрессирующего ожирения и диэнцефальной симптоматики.
ЭПИДЕМИОЛОГИЯ
Частота данной патологии составляет в популяции до 15–20%, примерно 30–35% в структуре нарушений репродуктивной функции и до 70% среди женщин с рецидивирующими гиперпластическими процессами эндометрия; частота ранних потерь беременности при данном синдроме возрастает до 35%.
ЭТИОЛОГИЯ
Причины развития метаболического синдрома - воздействие различных факторов (психические стрессы, нейроинфекции, различные операции, травмы, роды, аборты и др.) у женщин с определённым преморбидным фоном (врождённая или приобретённая функциональная лабильность гипоталамических и экстрагипоталамических структур).
ПАТОГЕНЕЗ
Первично происходит нарушение нейроэндокринной регуляции гипоталамуса, поэтому отмечается множество диэнцефальных симптомов (нарушение сна, аппетита, жажда, головокружения, головные боли, гипертензия и др.), указывающих на центральный (гипоталамический) генез данной патологии. В ответ на воздействие различных этиологических факторов (стресс) в экстрагипоталамических структурах мозга происходит нарушение обмена нейромедиаторов, в частности увеличение синтеза и выделения β-эндорфина и уменьшение продукции допамина.
Вследствие этого повышается секреция АКТГ, пролактина, нарушается цирхоральный ритм выделения гонадолиберина и, соответственно, гонадотропинов в гипофизе. Внегонадно синтезирующийся из андрогенов эстрон повышает чувствительность гипофиза к гонадолиберину, что дополнительно нарушает функцию гипоталамо-гипофизарно-яичниковой системы с формированием вторичных поликистозных яичников. Нарушения в системе гипоталамус-гипофиз-надпочечники. В ответ на избыточную стимуляцию АКТГ в надпочечниках повышается образование всех стероидных гормонов коры: глюкокортикоидов (кортизол), минералокортикоидов (альдостерон) и половых гормонов, в основном андрогенов. Гиперкортицизм способствует специфическому, так называемому висцеральному ожирению (центральное, кушингоидное, мужское, андроидное ожирение) с преимущественным отложением жировой ткани в области плечевого пояса, живота и мезентерия внутренних органов.
Висцеральная жировая ткань приводит к формированию инсулинорезистентности вследствие гиперинсулинемии. Затем происходит нарушение липидного спектра крови (дислипидемия), характеризующаяся повышением уровня атерогенных факторов (триглицеридов, липопротеидов низкой плотности, липопротеидов очень низкой плотности) и снижением уровня липопротеидов высокой плотности, что приводит к атеросклерозу и артериальной гипертонии. При этом последовательность развития метаболических нарушений соответствует длительности заболевания. Поэтому артериальная гипертония, обязательный компонент метаболического синдрома, проявляется, как правило, после 35 лет.
Висцеральному ожирению также способствует булимия (повышенный аппетит и избыточное потребление пищи) вследствие нарушения нейромедиаторного контроля за функцией центров пищевого поведения, находящихся в гипоталамусе. Периферической инсулинорезистентности также способствуют надпочечниковые андрогены и тестостерон, продуцирующийся в жировой ткани. Известно, что андрогены изменяют структуру мышечной ткани в сторону превалирования мышечных волокон II типа, менее чувствительных к инсулину. Таким образом, в результате активации оси «гипоталамус-гипофиз-надпочечники» формируются 4 основные компонента («смертельный квартет») метаболического синдрома: висцеральное ожирение, инсулинорезистентность, дислипидемия и артериальная гипертония.
Чёткой классификации и стадийности метаболического синдрома не существует. Несмотря на это, выраженность симптомов, количество компонентов синдрома Reaven и наличие осложнений оказывают влияние на стратификацию риска и выбор тактики лечения у конкретного пациента. Для этого следует учитывать:
• степень ожирения и артериальной гипертензии;
• выраженность метаболических изменений;
• наличие или отсутствие сахарного диабета и заболеваний, связанных с атеросклерозом.
В зависимости от индекса массы тела (ИМТ), который рассчитывается делением веса (кг) на рост (м2), классифицируются следующие типы массы тела (МТ):
• нормальная МТ — ИМТ ≥18,5 <25;
• избыточная МТ — ≥25 <30;
• ожирение I степени — ≥30 <35;
• ожирение II степени — ≥35 <40;
• ожирение III степени — ≥40.
ИМТ <18,5 характеризуется как дефицит массы тела.
Важную роль играет распределение жировой ткани. Различают два типа ожирения:
• гиноидный (по типу «груша»), когда избыточная жировая ткань распределяется преимущественно на бёдрах и ягодицах;
• андроидный (по типу «яблоко»; абдоминальное ожирение), с преимущественной локализацией жира в области верхней половины тела (живот, грудь, плечи, спина).
Второй тип ожирения является более патогенным в плане риска возникновения сердечно-сосудистых заболеваний и сахарного диабета. Это связано с ожирением внутренних органов, в том числе печени (висцеральное ожирение, неалкогольная жировая болезнь печени), снижением сатурации крови кислородом из-за перехода дыхания на грудной, поверхностный тип и эндокринной активностью висцеральной жировой ткани с патологическим изменением выработки адипокинов (лептин, грелин, адипонектин). Выявлена чёткая корреляция между увеличением абдоминальной жировой ткани и индекса массы тела с риском сопутствующих заболеваний. Считается, что риски начинают нарастать при увеличении окружности талии (ОТ) >80 см у женщин и 94 см у мужчин, а при ОТ >88 см и 102 см соответственно риск возрастает значительно.
Центральным патологическим звеном метаболического синдрома является изменение углеводного обмена. Концентрацию глюкозы оценивают в капиллярной крови (норма <5,6) и в венозной плазме (норма <6,1) натощак в ммоль/л. Гипергликемией натощак считается показатель ≥5,6 <6,1 и ≥6,1; <7,0; сахарный диабет — ≥6,1 и ≥6,1 <7,0, соответственно. Через 2 часа после углеводной нагрузки (75 гр глюкозы или 125 гр сахара рафинада, растворённых в 200 мл воды) нормальный показатель концентрации глюкозы в капиллярной и венозной крови — <7,8 ммоль/л; НТГ — ≥7,8 <11,1 и сахарный диабет — ≥11,1.
Ещё один важный компонент метаболического синдрома — артериальная гипертензия, которая может носить вторичный характер. Нормальным считается систолическое артериальное давление (САД) 120-129 мм рт.ст и диастолическое артериальное давление (ДАД) 80-84 мм рт.ст. САД <120 и ДАД <80 называют оптимальным давлением, а САД 130-139 и ДАД 85-89 — высоким нормальным артериальным давлением.
Различают три степени артериальной гипертензии:
• 1 ст. – САД 140-159, ДАД 90-99;
• 2 ст. - САД 160-179, ДАД 100-109;
• 3 ст. - САД ≥180, ДАД ≥110.
Повышение артериального давления характеризуется повышением риска сердечно-сосудистых событий. Для метаболического синдрома характерны также изменения липидного обмена, которые классифицированы в таблице ниже (в ммоль/л).
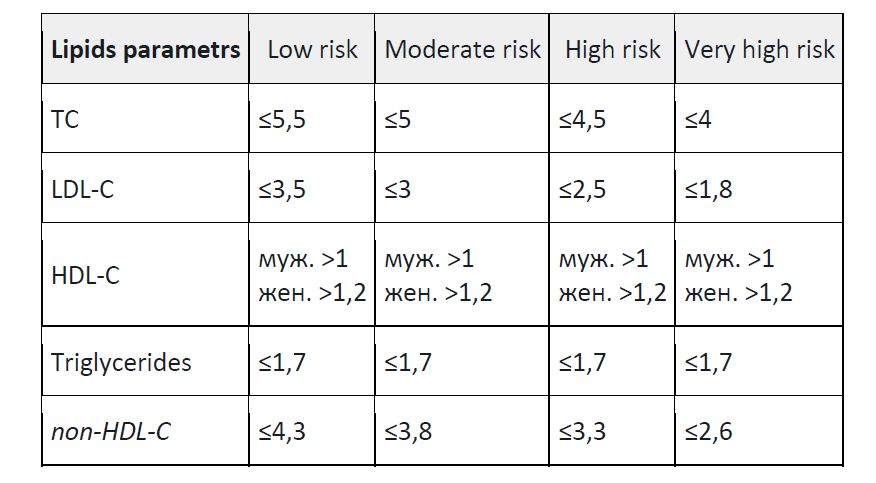
Note:
TC - total cholesterol;
LDL-C, low-density lipoprotein cholesterol;
HDL-C, high-density lipoprotein cholesterol;
non-HDL-C, non-high-density lipoprotein cholesterol.
high-density lipoproteins.
Роль инсулина в овариальной функции у женщин сводится к усилению ЛГ- зависимого синтеза тестостерона. Кроме того, инсулин подавляет продукцию ГСПГ (глобулин, связывающий половые гормоны) в печени, тем самым, повышая в крови уровень биологически активных свободных фракций тестостерона и эстрадиола. Гиперинсулинемия снижает продукцию в печени протеинов, связывающих инсулиноподобный фактор роста, что приводит к повышению биодоступности инсулиноподобного фактора роста, который, как и инсулин, усиливает синтез андрогенов в тека-клетках яичников. Все эти механизмы в конечном счёте усугубляют гиперандрогению.
Гипоталамо-гипофизарно-яичниковая система. У женщин с метаболическим синдромом поликистозные яичники формируются не только вследствие метаболических нарушений, но и первичного нарушения нейромедиаторного контроля за функцией гонадолиберина. Механизмы формирования вторичных поликистозных яичников можно упрощённо представить следующим образом. В результате изменения секреции гонадолиберина нарушается продукция гонадотропинов в сторону повышения уровня ЛГ и относительного снижения синтеза ФСГ. В яичниках нарушается процесс овуляции, происходит сначала персистенция фолликулов, затем их атрезия. В атретичных фолликулах продуцируется избыток андрогенов и происходит дефицит эстрадиола. По механизмам отрицательной обратной связи снижение концентрации эстрадиола стимулирует избыточную продукцию ЛГ. Яичниковые андрогены усугубляют процесс кистозной атрезии фолликулов, способствуют гиперплазии тека-клеток и стромы, а также утолщению белочной оболочки яичников. Избыток андрогенов первично из надпочечников, а затем из поликистозных яичников в жировой ткани увеличивает синтез эстрона. Большие концентрации внегонадного эстрона повышают чувствительность гипофиза к гонадолиберину, что приводит к хронической гиперсекреции ЛГ и замыкает «порочный круг» в формировании
вторичных поликистозных яичников.
КЛИНИЧЕСКАЯ КАРТИНА
Кардинальный признак метаболического синдрома у женщин — нарушение менструальной и генеративной функции на фоне прибавки массы тела на 10–30 кг. В основном пациентки жалуются на нарушение менструального цикла, невынашивание беременности, бесплодие, избыточное оволосение, ожирение и многообразие «диэнцефальных жалоб». Причем избыточную массу тела пациентки связывают с эндокринными нарушениями, а не с алиментарными факторами. Только при тщательно собранном анамнезе можно выявить наличие повышенного аппетита — основного фактора ожирения. У мужчин метаболический синдром часто развивается после 45 лет из-за снижения уровня тестостерона. На фоне дефицита гормоны увеличивается вес, нарушается метаболизм инсулина, повышается артериальное давление.
К последствиям метаболического синдрома у мужчин можно отнести:
• Атеросклеротическое поражение сосудов
• Ожирение
• Преддиабет
• Эректильная дисфункция. Патология вызвана атеросклеротическим поражением сосудов и артерий, подпитывающих яички и предстательную железу. У мужчин это выражается в снижении продолжительности эрекции, раннем семяизвержении, потере чувствительности головки полового члена. В Европе нормальным считается у людей старше 60 лет 1-2 половых акта в неделю. Многие возрастные пары после 40 занимаются сексом несколько раз в месяц. При этом качество секса не оставляет удовлетворения, провоцируя недовольство семейной жизнью и партнёром.
• Рак предстательной железы. Простата выполняет ряд функций: удерживает мочу, вырабатывает эякулят, перерабатывает тестостерон. При нехватке гормона клетки бездействуют и со временем мутируют. Избыток тестостерона также негативно сказывается на предстательной железе, и тоже провоцирует рак. Но раковые клетки в последнем случае менее агрессивны, и после операции и химиотерапии пациент имеет большие шансы полного выздоровления. При дефиците тестостерона мутировавшие клетки быстро дают метастазы и практически не поддаются химиотерапии).
• Остеопороз и хрупкость костей. Тестостерон влияет на плотность костей. Гормон провоцирует выработку остеобластов — молодых клеток костной ткани. Он также поддерживает минеральный состав костей. При снижении тестостерона возникает риск переломов, костная ткань становится более пористой.
Лишний холестерин, образуемый из-за снижения выработки тестостерона, оседает на сосудах сердца и головного мозга. Смерть после сердечного приступа молодого мужчины в 30-35 лет становится шоком для его родственников. Метаболический синдром и раннее снижение андрогенных гормонов часто имеет наследственный характер, поэтому его можно предсказать и вылечить.
ДИАГНОСТИКА
Диагностика метаболического синдрома основывается на данных клиники и фенотипических особенностей (нарушение менструального цикла, на фоне прибавки массы тела, андроидное ожирение и «диэнцефальные» жалобы).
АНАМНЕЗ
Из перенесённых заболеваний отмечается большая частота ОРВИ различной экстрагенитальной патологии. Наследственность у большинства пациентов отягощена нарушениями репродуктивной функции, ожирением, инсулиннезависимым сахарным диабетом, сердечно-сосудистыми заболеваниями. При этом необходимо выявить факторы, способствующие прибавке массы тела, для определения длительности заболевания и вероятности формирования вторичных признаков.
Менструальная и генеративная функция у женщин: возраст менархе не отличается от такового в популяции — 12–13 лет. Отличительный признак — вторичное нарушение менструального цикла после воздействия различных факторов на фоне прибавки массы тела. Нарушение менструального цикла начинается с увеличения длительности цикла, НЛФ (недостаточность лютеиновой фазы), а затем развивается олигоаменорея и хроническая ановуляция; частота дисфункциональных маточных кровотечений — до 20%. Поскольку у большинства пациенток в анамнезе были беременности, закончившиеся родами, абортами, нарушение генеративной функции чаще характеризуется вторичным бесплодием или невынашиванием беременности (в начале заболевания).
ФИЗИКАЛЬНОЕ ИССЛЕДОВАНИЕ
При физикальном исследовании — индекс массы тела соответствует ожирению и составляет свыше 30, а соотношение окружности талии к окружности бёдер характерно для висцерального типа ожирения (более 0,85). Важный клинический признак — полосы растяжения на коже живота, бёдер, от бледно-розового до багрового цвета. Часто наблюдают изменения кожи по типу «нигроидного акантоза», в виде шероховатых пигментированных участков кожи в местах трения и складок (паховые, подмышечные, под молочными железами, на животе). Эти изменения кожи свидетельствуют об инсулинорезистентности. Степень выраженности гирсутизма, угревой сыпи у женщин выше, чем при СПКЯ, что обусловлено влиянием не только надпочечниковых андрогенов, но и внегонадно синтезируемого тестостерона в большом количестве жировой ткани. При формировании вторичных поликистозных яичников усиливается рост стержневых волос не только по белой линии живота, околососковых полей и внутренней поверхности бёдер, но и часто в области подбородка, бакенбард, на грудине, спине, ягодицах. При этом у некоторых пациенток имеются признаки вирильного синдрома — андрогензависимая алопеция и снижение тембра голоса. Состояние молочных желёз характеризуется их гипертрофией за счёт жировой ткани и большой частотой фиброзно-кистозной мастопатии. При гинекологическом исследовании необходимо обратить внимание на степень эстрогенной насыщенности по цервикальному числу, которое на первой фазе заболевания составляет 10–12 см, а при формировании вторичных поликистозных яичников — 5–6 см. Кроме того, у этих пациенток «нигроидный акантоз» наиболее часто наблюдают в паховых складках. Помимо абдоминального ожирения, для постановки диагноза, необходимо иметь хотя бы два дополнительных критерия:
• артериальную гипертензию (артериальное давление ?140/90 мм рт.ст.);
• липидные показатели (ммоль/л) — повышение концентрации в крови триглицеридов ?1,7; снижение ХС ЛПВП <1,0 у мужчин; <1,2 у женщин и повышение ХС ЛПНП >3,0;
• углеводные показатели (ммоль/л) — гипергликемия натощак ?6,1 и НТГ 7,8 – <11,1
В клинических условиях нужно дифференцировать метаболический синдром от механического сочетания факторов риска, например артериальной гипертензии, избыточной массы тела без признаков абдоминального ожирения и повышения уровня общего холестерина крови, что встречается довольно часто (до 30%). В сомнительных случаях рекомендовано дополнительное определение инсулинорезистентности по следующим методикам:
• оценка базальной гиперинсулинемии в крови натощак (гиперинсулинемия — >18 мкед/мл);
• показатель HOMA-IR — произведение значения инсулина натощак (мкед/мл) на величину
глюкозы (ммоль/л), разделить на 22,5 (значение большее, чем 27, считается инсулинорезистентностью);
• индекс Caro — соотношение тощаковой глюкозы (в ммоль/л) к инсулину (в мкед/мл)
(инсулинорезистентность – значение < 0,33)
ИНСТРУМЕНТАЛЬНЫЕ ИССЛЕДОВАНИЯ
Метаболические нарушения характеризуются инсулинорезистентностью и, как следствие, гиперинсулинемией, дислипидемией (повышение липопротеидов низкой плотности, триглицеридов, снижение уровня липопротеидов высокой плотности). Пероральный глюкозотолерантный тест с определением базальных и стимулированных глюкозой концентраций инсулина и глюкозы выявляет нарушение толерантности к глюкозе. Пик инсулинемии наблюдается через 60 мин, а через 120 мин показатели инсулина (но не глюкозы) приходят к исходным или незначительно превышающим референтные значениям. Кроме того, лабораторными критериями инсулинорезистентности является концентрация базального инсулина 12,2 мМЕ/л и более. Информативным также можно считать определение индекса HOMA, значение которого более 2,5 свидетельствует об инсулинорезистентности. Для подсчёта данного индекса необходимы только значения базальных концентраций глюкозы и инсулина, которые перемножаются и делятся на 22,5.
Трансвагинальная эхография у женщин поможет выявить вторичные поликистозные яичники. В начале заболевания определяются мультифолликулярные яичники, которые отличаются нормальным объёмом стромы с множеством фолликулов до 10– 12 мм в диаметре.
ЛАБОРАТОРНЫЕ ИССЛЕДОВАНИЯ
Гормональные исследования характеризуются повышением в крови концентрации АКТГ, кортизола, пролактина. Уровень ЛГ и ФСГ может быть нормальным, а при формировании вторичных поликистозных яичников у женщин повышается концентрация ЛГ с увеличением соотношения ЛГ/ФСГ до 2,5–3. Также повышен уровень инсулина и снижен — ГСПГ (глобулин, связывающий половые гормоны). Кроме того, характерно увеличение содержания в крови 17-ОП, тестостерона и ДГЭАС. Это зачастую приводит к необоснованному назначению дексаметазона по поводу надпочечниковой гиперандрогении, что при гиперкортицизме патогенетически не обосновано, поскольку у этих пациенток и так повышена концентрация кортизола. При биопсии эндометрия отмечают большую частоту гиперпластических процессов и аденоматоза в эндометрии (до 60%), что, несомненно, связано с выраженными метаболическими нарушениями. Поэтому практикующие врачи должны относиться к этим пациенткам с онкологической настороженностью и рекомендовать раздельное выскабливание при нарушениях менструального цикла, а также эхографических признаках гиперплазии эндометрия.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
Дифференциальную диагностику проводят прежде всего с болезнью Кушинга. В диагностике необходимо участие общих эндокринологов, для которых болезнь Кушинга не редкость. При этом отмечаются высокие уровни АКТГ, кортизола и пролактина и эхографические признаки гиперплазии коры надпочечников. Дифференциальную диагностику у женщин также проводят с особой патологией яичников — стромальным текаматозом. Клиническая картина этой патологии характеризуется ожирением, выраженным вирильным синдромом с «нигроидным акантозом» и инсулинорезистентностью. В крови значительно повышен уровень андрогенов при нормальном содержании ЛГ и ФСГ, размеры яичников могут быть нормальными. Характерный признак — рецидивирующие гиперпластические процессы эндометрия, не поддающиеся гормонотерапии. Наиболее часто приходится проводить дифференциальную диагностику с СПКЯ и ожирением. При этом основная роль отводится данным анамнеза (вторичности нарушений менструальной и генеративной функции на фоне метаболического синдрома), поскольку при формировании вторичных поликистозных яичников эхографические, эндокринологические и метаболические характеристики не отличаются от таковых при СПКЯ с ожирением.
ЛЕЧЕНИЕ
Лечение представляет определённые трудности, поскольку восстановления гормональной и генеративной функции можно добиться только на фоне нормализации массы тела. Наиболее частая ошибка практикующих врачей — гормонотерапия на фоне ожирения. Важно раннее выявление заболевания на стадии функциональных нарушений, до формирования серьезных осложнений. В этом случае метаболическая терапия приводит к восстановлению нормального артериального давления, нормализации показателей крови, восстановлению репродуктивной и сексуальной функции у пациентов обоих полов.
ЦЕЛИ ЛЕЧЕНИЯ
Основная цель лечения — нормализация массы тела, восстановление метаболического и гормонального гомеостаза, что способствует не только реализации генеративной функции, но и снижению риска для здоровья, выработке долговременных навыков здорового образа жизни. Рациональное питание подразумевает снижение энергетической ценности за счёт жиров и углеводов и лежит в основе метаболической терапии. Длительность метаболической терапии — 6 и более месяцев в зависимости от исходной массы тела и темпов её снижения.
После снижения массы тела у части женщин восстанавливается овуляторный менструальный цикл и фертильность, так как ещё не сформировались вторичные поликистозные яичники. На период нормализации массы тела рекомендуется предохранение от беременности, которая может осложниться тяжёлым гестозом или прерваться на ранних сроках. Ановуляция после нормализации массы тела и метаболических нарушений указывает на формирование вторичных поликистозных яичников. В этом случае рекомендуют стимуляцию овуляции консервативным или хирургическим путём. Поскольку бесплодие чаще вторичное, перед проведением стимуляции овуляции обязательно исключение трубного фактора.
Многофакторный патогенез метаболического синдрома с вовлечением многих систем в организме обусловливает сложность и малую эффективность терапии, основой которой должна быть регуляция нейромедиаторного обмена ЦНС на фоне нормализации массы тела, особенно при формировании осложнений. Своевременная коррекция метаболических нарушений на первой (функциональной) стадии заболевания более эффективна в восстановлении репродуктивного здоровья и профилактике развития сердечнососудистых заболеваний, инсулинонезависимого сахарного диабета — последствий метаболического синдрома, ухудшающих качество жизни людей.
www.SmartHealth.clinic
TC - total cholesterol;
LDL-C, low-density lipoprotein cholesterol;
HDL-C, high-density lipoprotein cholesterol;
non-HDL-C, non-high-density lipoprotein cholesterol.
high-density lipoproteins.
Роль инсулина в овариальной функции у женщин сводится к усилению ЛГ- зависимого синтеза тестостерона. Кроме того, инсулин подавляет продукцию ГСПГ (глобулин, связывающий половые гормоны) в печени, тем самым, повышая в крови уровень биологически активных свободных фракций тестостерона и эстрадиола. Гиперинсулинемия снижает продукцию в печени протеинов, связывающих инсулиноподобный фактор роста, что приводит к повышению биодоступности инсулиноподобного фактора роста, который, как и инсулин, усиливает синтез андрогенов в тека-клетках яичников. Все эти механизмы в конечном счёте усугубляют гиперандрогению.
Гипоталамо-гипофизарно-яичниковая система. У женщин с метаболическим синдромом поликистозные яичники формируются не только вследствие метаболических нарушений, но и первичного нарушения нейромедиаторного контроля за функцией гонадолиберина. Механизмы формирования вторичных поликистозных яичников можно упрощённо представить следующим образом. В результате изменения секреции гонадолиберина нарушается продукция гонадотропинов в сторону повышения уровня ЛГ и относительного снижения синтеза ФСГ. В яичниках нарушается процесс овуляции, происходит сначала персистенция фолликулов, затем их атрезия. В атретичных фолликулах продуцируется избыток андрогенов и происходит дефицит эстрадиола. По механизмам отрицательной обратной связи снижение концентрации эстрадиола стимулирует избыточную продукцию ЛГ. Яичниковые андрогены усугубляют процесс кистозной атрезии фолликулов, способствуют гиперплазии тека-клеток и стромы, а также утолщению белочной оболочки яичников. Избыток андрогенов первично из надпочечников, а затем из поликистозных яичников в жировой ткани увеличивает синтез эстрона. Большие концентрации внегонадного эстрона повышают чувствительность гипофиза к гонадолиберину, что приводит к хронической гиперсекреции ЛГ и замыкает «порочный круг» в формировании
вторичных поликистозных яичников.
КЛИНИЧЕСКАЯ КАРТИНА
Кардинальный признак метаболического синдрома у женщин — нарушение менструальной и генеративной функции на фоне прибавки массы тела на 10–30 кг. В основном пациентки жалуются на нарушение менструального цикла, невынашивание беременности, бесплодие, избыточное оволосение, ожирение и многообразие «диэнцефальных жалоб». Причем избыточную массу тела пациентки связывают с эндокринными нарушениями, а не с алиментарными факторами. Только при тщательно собранном анамнезе можно выявить наличие повышенного аппетита — основного фактора ожирения. У мужчин метаболический синдром часто развивается после 45 лет из-за снижения уровня тестостерона. На фоне дефицита гормоны увеличивается вес, нарушается метаболизм инсулина, повышается артериальное давление.
К последствиям метаболического синдрома у мужчин можно отнести:
• Атеросклеротическое поражение сосудов
• Ожирение
• Преддиабет
• Эректильная дисфункция. Патология вызвана атеросклеротическим поражением сосудов и артерий, подпитывающих яички и предстательную железу. У мужчин это выражается в снижении продолжительности эрекции, раннем семяизвержении, потере чувствительности головки полового члена. В Европе нормальным считается у людей старше 60 лет 1-2 половых акта в неделю. Многие возрастные пары после 40 занимаются сексом несколько раз в месяц. При этом качество секса не оставляет удовлетворения, провоцируя недовольство семейной жизнью и партнёром.
• Рак предстательной железы. Простата выполняет ряд функций: удерживает мочу, вырабатывает эякулят, перерабатывает тестостерон. При нехватке гормона клетки бездействуют и со временем мутируют. Избыток тестостерона также негативно сказывается на предстательной железе, и тоже провоцирует рак. Но раковые клетки в последнем случае менее агрессивны, и после операции и химиотерапии пациент имеет большие шансы полного выздоровления. При дефиците тестостерона мутировавшие клетки быстро дают метастазы и практически не поддаются химиотерапии).
• Остеопороз и хрупкость костей. Тестостерон влияет на плотность костей. Гормон провоцирует выработку остеобластов — молодых клеток костной ткани. Он также поддерживает минеральный состав костей. При снижении тестостерона возникает риск переломов, костная ткань становится более пористой.
Лишний холестерин, образуемый из-за снижения выработки тестостерона, оседает на сосудах сердца и головного мозга. Смерть после сердечного приступа молодого мужчины в 30-35 лет становится шоком для его родственников. Метаболический синдром и раннее снижение андрогенных гормонов часто имеет наследственный характер, поэтому его можно предсказать и вылечить.
ДИАГНОСТИКА
Диагностика метаболического синдрома основывается на данных клиники и фенотипических особенностей (нарушение менструального цикла, на фоне прибавки массы тела, андроидное ожирение и «диэнцефальные» жалобы).
АНАМНЕЗ
Из перенесённых заболеваний отмечается большая частота ОРВИ различной экстрагенитальной патологии. Наследственность у большинства пациентов отягощена нарушениями репродуктивной функции, ожирением, инсулиннезависимым сахарным диабетом, сердечно-сосудистыми заболеваниями. При этом необходимо выявить факторы, способствующие прибавке массы тела, для определения длительности заболевания и вероятности формирования вторичных признаков.
Менструальная и генеративная функция у женщин: возраст менархе не отличается от такового в популяции — 12–13 лет. Отличительный признак — вторичное нарушение менструального цикла после воздействия различных факторов на фоне прибавки массы тела. Нарушение менструального цикла начинается с увеличения длительности цикла, НЛФ (недостаточность лютеиновой фазы), а затем развивается олигоаменорея и хроническая ановуляция; частота дисфункциональных маточных кровотечений — до 20%. Поскольку у большинства пациенток в анамнезе были беременности, закончившиеся родами, абортами, нарушение генеративной функции чаще характеризуется вторичным бесплодием или невынашиванием беременности (в начале заболевания).
ФИЗИКАЛЬНОЕ ИССЛЕДОВАНИЕ
При физикальном исследовании — индекс массы тела соответствует ожирению и составляет свыше 30, а соотношение окружности талии к окружности бёдер характерно для висцерального типа ожирения (более 0,85). Важный клинический признак — полосы растяжения на коже живота, бёдер, от бледно-розового до багрового цвета. Часто наблюдают изменения кожи по типу «нигроидного акантоза», в виде шероховатых пигментированных участков кожи в местах трения и складок (паховые, подмышечные, под молочными железами, на животе). Эти изменения кожи свидетельствуют об инсулинорезистентности. Степень выраженности гирсутизма, угревой сыпи у женщин выше, чем при СПКЯ, что обусловлено влиянием не только надпочечниковых андрогенов, но и внегонадно синтезируемого тестостерона в большом количестве жировой ткани. При формировании вторичных поликистозных яичников усиливается рост стержневых волос не только по белой линии живота, околососковых полей и внутренней поверхности бёдер, но и часто в области подбородка, бакенбард, на грудине, спине, ягодицах. При этом у некоторых пациенток имеются признаки вирильного синдрома — андрогензависимая алопеция и снижение тембра голоса. Состояние молочных желёз характеризуется их гипертрофией за счёт жировой ткани и большой частотой фиброзно-кистозной мастопатии. При гинекологическом исследовании необходимо обратить внимание на степень эстрогенной насыщенности по цервикальному числу, которое на первой фазе заболевания составляет 10–12 см, а при формировании вторичных поликистозных яичников — 5–6 см. Кроме того, у этих пациенток «нигроидный акантоз» наиболее часто наблюдают в паховых складках. Помимо абдоминального ожирения, для постановки диагноза, необходимо иметь хотя бы два дополнительных критерия:
• артериальную гипертензию (артериальное давление ?140/90 мм рт.ст.);
• липидные показатели (ммоль/л) — повышение концентрации в крови триглицеридов ?1,7; снижение ХС ЛПВП <1,0 у мужчин; <1,2 у женщин и повышение ХС ЛПНП >3,0;
• углеводные показатели (ммоль/л) — гипергликемия натощак ?6,1 и НТГ 7,8 – <11,1
В клинических условиях нужно дифференцировать метаболический синдром от механического сочетания факторов риска, например артериальной гипертензии, избыточной массы тела без признаков абдоминального ожирения и повышения уровня общего холестерина крови, что встречается довольно часто (до 30%). В сомнительных случаях рекомендовано дополнительное определение инсулинорезистентности по следующим методикам:
• оценка базальной гиперинсулинемии в крови натощак (гиперинсулинемия — >18 мкед/мл);
• показатель HOMA-IR — произведение значения инсулина натощак (мкед/мл) на величину
глюкозы (ммоль/л), разделить на 22,5 (значение большее, чем 27, считается инсулинорезистентностью);
• индекс Caro — соотношение тощаковой глюкозы (в ммоль/л) к инсулину (в мкед/мл)
(инсулинорезистентность – значение < 0,33)
ИНСТРУМЕНТАЛЬНЫЕ ИССЛЕДОВАНИЯ
Метаболические нарушения характеризуются инсулинорезистентностью и, как следствие, гиперинсулинемией, дислипидемией (повышение липопротеидов низкой плотности, триглицеридов, снижение уровня липопротеидов высокой плотности). Пероральный глюкозотолерантный тест с определением базальных и стимулированных глюкозой концентраций инсулина и глюкозы выявляет нарушение толерантности к глюкозе. Пик инсулинемии наблюдается через 60 мин, а через 120 мин показатели инсулина (но не глюкозы) приходят к исходным или незначительно превышающим референтные значениям. Кроме того, лабораторными критериями инсулинорезистентности является концентрация базального инсулина 12,2 мМЕ/л и более. Информативным также можно считать определение индекса HOMA, значение которого более 2,5 свидетельствует об инсулинорезистентности. Для подсчёта данного индекса необходимы только значения базальных концентраций глюкозы и инсулина, которые перемножаются и делятся на 22,5.
Трансвагинальная эхография у женщин поможет выявить вторичные поликистозные яичники. В начале заболевания определяются мультифолликулярные яичники, которые отличаются нормальным объёмом стромы с множеством фолликулов до 10– 12 мм в диаметре.
ЛАБОРАТОРНЫЕ ИССЛЕДОВАНИЯ
Гормональные исследования характеризуются повышением в крови концентрации АКТГ, кортизола, пролактина. Уровень ЛГ и ФСГ может быть нормальным, а при формировании вторичных поликистозных яичников у женщин повышается концентрация ЛГ с увеличением соотношения ЛГ/ФСГ до 2,5–3. Также повышен уровень инсулина и снижен — ГСПГ (глобулин, связывающий половые гормоны). Кроме того, характерно увеличение содержания в крови 17-ОП, тестостерона и ДГЭАС. Это зачастую приводит к необоснованному назначению дексаметазона по поводу надпочечниковой гиперандрогении, что при гиперкортицизме патогенетически не обосновано, поскольку у этих пациенток и так повышена концентрация кортизола. При биопсии эндометрия отмечают большую частоту гиперпластических процессов и аденоматоза в эндометрии (до 60%), что, несомненно, связано с выраженными метаболическими нарушениями. Поэтому практикующие врачи должны относиться к этим пациенткам с онкологической настороженностью и рекомендовать раздельное выскабливание при нарушениях менструального цикла, а также эхографических признаках гиперплазии эндометрия.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
Дифференциальную диагностику проводят прежде всего с болезнью Кушинга. В диагностике необходимо участие общих эндокринологов, для которых болезнь Кушинга не редкость. При этом отмечаются высокие уровни АКТГ, кортизола и пролактина и эхографические признаки гиперплазии коры надпочечников. Дифференциальную диагностику у женщин также проводят с особой патологией яичников — стромальным текаматозом. Клиническая картина этой патологии характеризуется ожирением, выраженным вирильным синдромом с «нигроидным акантозом» и инсулинорезистентностью. В крови значительно повышен уровень андрогенов при нормальном содержании ЛГ и ФСГ, размеры яичников могут быть нормальными. Характерный признак — рецидивирующие гиперпластические процессы эндометрия, не поддающиеся гормонотерапии. Наиболее часто приходится проводить дифференциальную диагностику с СПКЯ и ожирением. При этом основная роль отводится данным анамнеза (вторичности нарушений менструальной и генеративной функции на фоне метаболического синдрома), поскольку при формировании вторичных поликистозных яичников эхографические, эндокринологические и метаболические характеристики не отличаются от таковых при СПКЯ с ожирением.
ЛЕЧЕНИЕ
Лечение представляет определённые трудности, поскольку восстановления гормональной и генеративной функции можно добиться только на фоне нормализации массы тела. Наиболее частая ошибка практикующих врачей — гормонотерапия на фоне ожирения. Важно раннее выявление заболевания на стадии функциональных нарушений, до формирования серьезных осложнений. В этом случае метаболическая терапия приводит к восстановлению нормального артериального давления, нормализации показателей крови, восстановлению репродуктивной и сексуальной функции у пациентов обоих полов.
ЦЕЛИ ЛЕЧЕНИЯ
Основная цель лечения — нормализация массы тела, восстановление метаболического и гормонального гомеостаза, что способствует не только реализации генеративной функции, но и снижению риска для здоровья, выработке долговременных навыков здорового образа жизни. Рациональное питание подразумевает снижение энергетической ценности за счёт жиров и углеводов и лежит в основе метаболической терапии. Длительность метаболической терапии — 6 и более месяцев в зависимости от исходной массы тела и темпов её снижения.
После снижения массы тела у части женщин восстанавливается овуляторный менструальный цикл и фертильность, так как ещё не сформировались вторичные поликистозные яичники. На период нормализации массы тела рекомендуется предохранение от беременности, которая может осложниться тяжёлым гестозом или прерваться на ранних сроках. Ановуляция после нормализации массы тела и метаболических нарушений указывает на формирование вторичных поликистозных яичников. В этом случае рекомендуют стимуляцию овуляции консервативным или хирургическим путём. Поскольку бесплодие чаще вторичное, перед проведением стимуляции овуляции обязательно исключение трубного фактора.
Многофакторный патогенез метаболического синдрома с вовлечением многих систем в организме обусловливает сложность и малую эффективность терапии, основой которой должна быть регуляция нейромедиаторного обмена ЦНС на фоне нормализации массы тела, особенно при формировании осложнений. Своевременная коррекция метаболических нарушений на первой (функциональной) стадии заболевания более эффективна в восстановлении репродуктивного здоровья и профилактике развития сердечнососудистых заболеваний, инсулинонезависимого сахарного диабета — последствий метаболического синдрома, ухудшающих качество жизни людей.
www.SmartHealth.clinic






